 埃默里 - 德赖富斯肌营养不良症是什么? 埃默里 - 德赖富斯肌营养不良症是什么?
【概述】
金刚砂Dreifuss肌营养不良症(EDMD)是肌营养不良症九种类型的一种,是一组遗传的退行性疾病,主要影响的自主肌肉。它被命名为艾伦·埃默里和弗里茨·德赖富斯,在20世纪60年代医生首先在弗吉尼亚州的家庭之间描述的障碍。Emery-Dreifuss肌营养不良是一种相对良性、儿童早期发病、缓慢进展的遗传性肌肉疾病,临床上少见。临床特点表现为早期出现关节挛缩,受累肌肉呈肱-腓分布并伴有心脏受累。智力不会受到影响。
EDMD什么症状?
EDMD往往在儿童期发病,通常10岁左右显示自身的特点肩膀和上臂和腿的小腿肌肉萎缩,使肌肉无力。另一个突出EDMD方面外观挛缩(关节僵硬),病程很早就在手肘、脖子和脚跟表现。最后非常重要的,称为传导阻滞的心脏问题是一个EDMD共同的特点和需要监控。
EDMD什么原因?
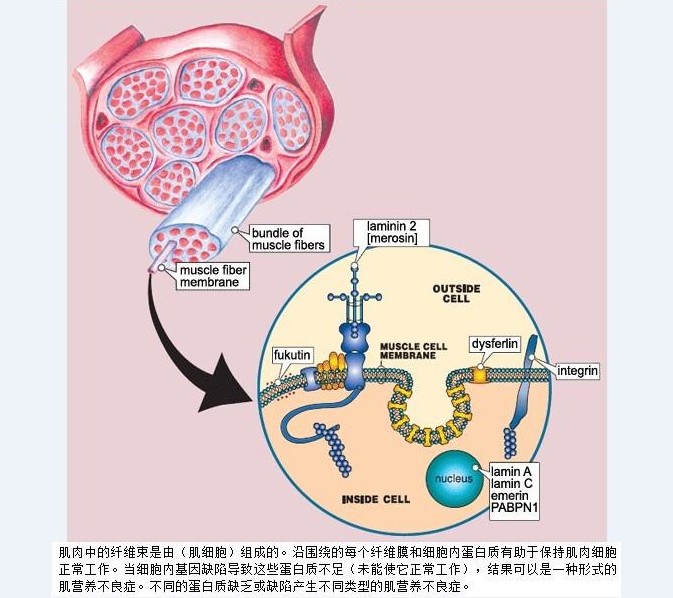
EDMD在每一块肌肉细胞的细胞周围的核膜产生的蛋白质的基因突变引起的。EDMD可以继承几种不同的方式,虽然症状基本上所有继承模式相同。
EDMD什么进展?
EDMD进展缓慢。肌肉无力,可能不会成为以后生活中的困难,智力不会受到影响。虽然心脏问题通常在20岁需要关注。
对EDMD状态什么研究?
研究人员已经确定的是基因出现故障,导致EDMD,科学家们对这些知识在以多种方式设想。研究EDMD包括基因和细胞方向。
症状和体征
埃默里 - 德赖富斯肌营养不良症(EDMD)的症状通常在10岁明显。早期迹象包括“因为脚跟肌腱跟腱的僵硬脚趾走态”和肘部弯曲困难。其他早期症状包括肩,上臂和小腿肌肉无力和萎缩。
发生早在EDMD挛缩(关节僵硬),可能会使手臂,颈部,脚后跟和脊柱运动困难。然而,肌肉无力的进展似乎发生在EDMD的速度非常缓慢,可能不会成为一个困难的来源,直到以后的生活中。
昏厥由于心脏异常,也可以是一个EDMD的早期迹象。通常情况下,心脏的问题20岁能检测到,但他们也可以发生在疾病的早期阶段。一些妇女如果是X-连锁遗传EDMD携带者也可能有心脏问题的风险,这种风险可能随着年龄的增加。(X-连锁EDMD携带者不倾向于有肌肉无力或挛缩。)
检查诊断
任何形式的肌营养不良症的诊断,医生通常开始由病人和家族病史进行体检。可以学到很多东西,这些包括弱点模式。很长的病史和物理走向作出诊断,甚至之前做过很多复杂的诊断测试。
医生也想确定是肌肉本身的问题,或是运动神经元的问题,可能会导致的弱点,看起来像一个肌肉问题,但真的不是。
通常情况下,疲软的起源可以针对体检。有时候,特殊的测试称为神经传导研究和肌电图(EMG)。在这些测试中,电力和非常精细的针脚用于刺激和评估的肌肉或神经,个别地看到了问题所在。肌电图是不舒服,但通常不会很痛苦。
开始诊断过程中医生常常采集特殊的血液测试,称为CK水平。对照肌酸激酶,肌肉受损泄漏的一种酶。CK水平升高时,血液样本中发现的,它通常意味着一些异常的过程中,如肌肉萎缩症或炎症,肌肉被破坏。因此,一个高的CK水平往往表明,肌肉本身的弱点是有可能的原因,但它并没有告诉正是肌症。患者血清CPK活性可增高至2~20倍,但年龄较大者则CPK多数正常。心电图检查见有各种心律不齐、房室传导阻滞、房室扩大以及心肌损害等。肌电图显示肌源性损害。
为了确定哪些障碍是造成,医生可能要肌肉活检,肌肉的手术切除病人的一个小样本。此示例通过检查,医生可以告诉肌肉内发生了什么变化。现代技术可以使用活检,以区别于肌营养不良症感染,炎症性疾病和其它问题。
活检样本的其他测试可以提供哪些肌肉蛋白是存在于肌肉细胞,无论他们是在正常的数额和在正确的位置信息。这可以告诉医生和病人,细胞的蛋白质有什么不对。
遗传基因(DNA)测试,使用血液样本,可以分析人的基因,特别是导致EDMD的缺陷,帮助预测疾病当然和帮助家庭下一代的疾病的风险评估,得到一个明确的基因诊断。
EDMD什么起因?
研究人员发现,当出现故障导致EDMD形式的基因。我们知道,这是在X染色体上EDMD缺陷的基因,使一个小的蛋白质称为emerin,通常位于在每个细胞的细胞核膜包围(在细胞的中心染色体包含)。
目前尚不了解如何在X染色体EDMD核膜中亏损emerin,导致肌肉萎缩的症状。一些研究人员认为,这种缺乏emerin干扰细胞分裂后核膜重组,导致的细胞弱或细胞死亡。沿着这些同样的思路,这是被发现在常染色体显性遗传和隐性形式的EDMD有缺陷的基因,包含两个密切相关的蛋白质的指令称为核纤层蛋白蛋白A和核纤层蛋白C的也都与细胞的核膜有关。然而,它还不知道emerin和C如何变化导致肌肉萎缩的症状,但一些研究表明,核膜emerin蛋白质异常时,可能成为不稳定因素,这可能会导致肌肉细胞分解。
有待回答的另一个问题是,emerin和核纤层蛋白在人体大多数组织发现,为什么EDMD症状限制主要是骨骼(自主)肌肉和心脏肌肉。
如何继承得到EDMD?
EDMD是最常见的继承,通过X-连锁隐性遗传模式,主要影响男性,继承了其母亲的基因。另一种形式是常染色体显性遗传,也就是说,它可以通过继承父母任何一方。第三,非常罕见的类型是常染色体隐性遗传,有缺陷的基因是从父母双方各继承一个。
【病因与发病机制】
EDMD是原发性进行性肌营养不良症的一个罕见类型。1966年Emery和Dreifuss将EDMD确定,1979年Rowland对该病进行了详细的阐述,其临床特征为:(1)早期出现肢体关节挛缩;(2)缓慢进展的肢体肌肉萎缩与无力;(3)心肌与心脏传导改变严重。1994年Bione证实EDMD基因;1999年确定常染色体显性遗传的EDMD基因是LMNA。EDMD的遗传方式多为性连锁隐性遗传和常染色体显性遗传,基因定位于第28对染色体长臂上(Xq28),基因调控产物为emerin蛋白,通常是女性携带,男性发病。但Emery(1987年)报道本病也有常染色体显性遗传形式。
EDMD存在两种主要的遗传方式。①X-连锁隐性遗传:该型致病基因定位于Xq28,基因全长2 100bp,包括6个外显子,编码762bp的mRNA。其34KD的蛋白产物由254个氨基酸构成,称为emerin。emerin是锚定于骨骼肌、心肌和平滑肌核膜内表面的核内膜蛋白,其主要功能是在肌肉收缩过程中对抗机械性压力以稳定核膜。目前已发现该基因有100种左右的突变形式,包括点突变、小片段缺失和无义突变等。②常染色体显性遗传:该类型的基因为LMNA,定位于Iq11-23,基因全长24kb,包含12个外显子。由于其10号外显子的不同剪接形式,产生两种不同的mRNA。一种为1 992bp的mRNA编码前体laminA(核纤层蛋白A);另一种为1 716bp的mRNA编码laminC(核纤层蛋白C)。lamin是核膜的组成部分,定位于核膜板层,它在DNA复制、染色体构建、核孔复合体的空间构形、细胞核发育、核膜蛋白锚定等方面起作用。迄今已经报道LMNA基因存在32种不同的突变形式。
|